 LE BRUNISSEMENT DES FRUITS
LE BRUNISSEMENT DES FRUITS
Le brunissement d’un fruit est un phénomène fréquent, se manifestant souvent après avoir découpé le fruit, et qui est très visible, notamment dans le cas de la pomme. Ce brunissement de la pomme est accompagné par la même occasion, et ce pour tous les fruits, d’une dégradation de l’odeur et du goût du fruit, une modification donc des qualités organoleptiques (un critère qui peut être apprécié par un des sens humains).
Ce brunissement du fruit est parfois souhaitable, notamment car il permet une amélioration du goût de certains aliments, mais il est aussi indésirable dans de nombreux cas, car l’aliment dépéri et n’est ainsi plus revendable. Ce phénomène peut cependant être évité, en comprenant tout d’abord son fonctionnement, et c’est ce que nous allons faire dans cette partie du TPE.
Le phénomène du brunissement du fruit trouve son origine première au sein des cellules du fruit, avec une enzyme, la polyphénoloxidase (abrégée PPO) qui va agir sur des composés chimiques appelés composés phénoliques, que nous réduirons au terme de phénols, un groupe d’espèces chimiques qui comportent un groupe caractéristique -OH (hydroxyle). Les phénols sont donc des alcools, et ceux-ci possèdent des propriétés aromatiques, à l’origine notamment en partie du goût des fruits. Ces 2 éléments sont communs à tous les fruits et légumes et expliquent par la suite le brunissement que l’on appellera alors “enzymatique”.
Souvent, on parle de l’oxydation d’un fruit en parlant en réalité du brunissement du fruit. Cela s’explique car le brunissement enzymatique nécessite la présence d’oxygène, contenu dans l’air sous forme de dioxygène, pour s’opérer, afin d’oxyder les phénols, selon la réaction d'oxydoréduction dont nous traiterons en première partie.
Dans un premier temps, nous introduirons donc la réaction d’oxydoréduction, nécessaire à la compréhension du brunissement enzymatique, puis, nous parlerons de l’oxydation des phénols contenus dans les fruits par l’air à l’origine du brunissement enzymatique, sous l’action de la polyphénoloxydase.
I. La réaction d’oxydoréduction : un élément nécessaire à la compréhension du brunissement enzymatique
1. L’oxydoréduction, réaction chimique de l’être vivant
Le brunissement des fruits fait intervenir l’oxydation d’espèces chimiques. Il s’agit d’une moitié de la réaction d’oxydoréduction (abrégée réaction redox), qui est commune à tous les êtres vivants, jouant notamment un rôle important dans la transformation du dioxygène de l’air, et qui a donc une place importante au sein de ceux-ci.
Dans le cas des fruits, les réactions redox auront un effet sur la transformation de l’oxygène au contact des phénols qui vont alors s’oxyder en quinones. C’est cette molécule qui constitue un élément principal de la phase finale du brunissement enzymatique, avant l’apparition de l’espèce colorée, la mélanine.
Cette réaction d’oxydoréduction fait toujours intervenir deux entités chimiques ioniques ou moléculaires, qui vont procéder à des échanges d'électrons : l’oxydant, et le réducteur. Pour que cette réaction ait lieu, il faut cependant présence d’atomes d’oxygène au sein de la réaction. (En effet, oxydation signifie combinaison avec l’oxygène).
Nous allons donc désormais décrire ce qu’est cette réaction.
La première entité qui intervient, l’oxydant, est susceptible de capter un ou plusieurs électrons selon la demi-équation (dite demi-équation d’oxydation) de forme Ox + ne- = Red. Dans cette demi-équation, Ox représente l’oxydant, et n un nombre réel, définissant le nombre d’électrons. A la fin de cette réaction entre l’oxydant et des électrons, on dira que l’oxydant a été réduit : On obtient alors le réducteur conjugué Red, qui peut par exemple être un ion ou un atome, selon la charge électrique initiale de l’oxydant.
Le réducteur est l’autre entité en jeu qui est susceptible quant à elle de céder un ou plusieurs électrons selon la demi-équation (dite de réduction cette fois ci) de forme Red + ne- = Ox. Les notations sont ici les mêmes que dans la réaction d’oxydation. A la suite de celle-ci, on dira que le réducteur a été oxydé par les électrons pour former l’oxydant conjugué Ox, une espèce électriquement chargé ou non selon la charge de départ du réducteur.
Ainsi, les réducteurs et les oxydants forment un couple, un ensemble, qui est susceptible de s’échanger un ou plusieurs électrons selon la demi-équation d’oxydoréduction de la forme :
Ox + ne- = Red
La réaction d’oxydoréduction complète correspond donc au transfert entre deux couples Ox1/Red1 et Ox2/Red2 d’électrons depuis le réducteur Red1 vers l’oxydant Ox2 qui va les capter. Ox2 a donc été réduit par Red1, ou on peut aussi dire que Red1 a été réduit par Ox2.
En milieu acide nous aurons donc finalement les deux demi-équation d’oxydoréduction de formes :
Ox1 + n1e- = Red1
Ox2 + n2e- = Red2
Et l’équation d’oxydoréduction finale regroupera ces deux demi-équations en une seule, donc la forme est :
n2 Ox1 + n1 Red1 -> n2 Red1 + n1 Ox2
Cette réaction s’applique ainsi au sein des fruits lors du brunissement de ceux-ci, les phénols jouant alors le rôle de réducteur, et l’oxygène le rôle de l’oxydant.
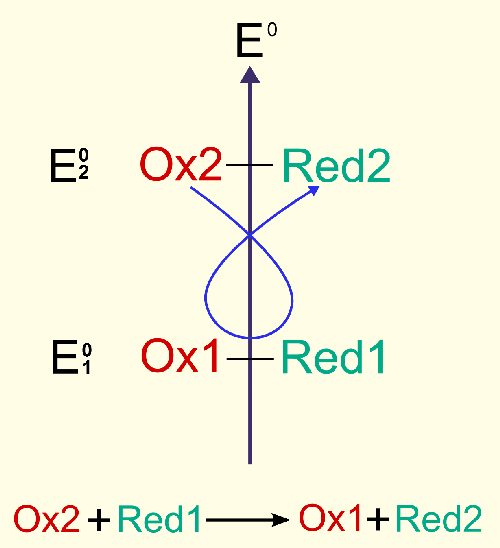 Ce schéma résume parfaitement la réaction d'oxydoréduction (redox). Deux couples Oxydant/Réducteur vont s'échanger des électrons.
Credit Photographique : Wikipédia [Lien]
Ce schéma résume parfaitement la réaction d'oxydoréduction (redox). Deux couples Oxydant/Réducteur vont s'échanger des électrons.
Credit Photographique : Wikipédia [Lien]
2. Les radicaux libres
L’oxygène joue donc un rôle important sur les aliments en général. On dit en effet souvent que celui-ci attaque l’aliment. Cependant, pour comprendre ce concept, il faut s’intéresser aux radicaux libres, les espèces responsables de cette détérioration du fruit.
A la suite de ces réactions d’oxydation, des espèces appelées radicaux libres se forment, et constituent les “déchets” de cette réaction. Ces espèces possèdent des électrons qui ne sont pas raccrochés à la couche externe de l’atome. On parle alors d’électron célibataire. Puisque les électrons sont toujours en couple dans la nature, cette espèce est alors très instable, et va ainsi essayer d’arracher un électron à d’autres couples d’électrons qu’elle rencontre sur d’autres entités pour redevenir stable.
Mais maintenant que cette première entité est stable, elle entraîne une réaction en chaîne. En effet, un nouveau radical libre va se former à chaque fois qu’une entité instable récupère un électron sur une entité stable, puisque celui-ci aura perdu un électron. Ce nouveau radical libre suivra alors les mêmes étapes que le précédent. Il récupérera un électron et formera un nouveau radical libre, d’où le terme de réaction en chaîne, un élément déclencheur initial provoquant alors une succession des mêmes réactions.
Ces réactions en chaîne causent alors le vieillissement des cellules du fruit, car ces radicaux libres attaquent les membres cellulaires notamment, pour regagner leur stabilité. On retrouve notamment ce même processus chez l’Homme.
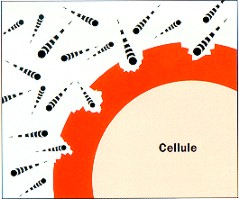 Ce schéma illustre l'action des radicaux libres sur la membrane des cellules. On voit bien que la membrane est détériorée par l'action des radicaux libres qui cherchent à se stabiliser.
Credit Photographique : www.immortalite8.wordpress.com/ [Lien]
Ce schéma illustre l'action des radicaux libres sur la membrane des cellules. On voit bien que la membrane est détériorée par l'action des radicaux libres qui cherchent à se stabiliser.
Credit Photographique : www.immortalite8.wordpress.com/ [Lien]
Ainsi, une réaction qui est nécessaire à la vie - car l’oxydation joue un rôle essentiel dans la respiration ou d’autres métabolismes cellulaires - se révèle un danger d’autre part. En effet, lors de la respiration, environ 5% du dioxygène consommé conduira à la formation de radicaux libres. C’est donc cette production constante de radicaux libres qui va mener au vieillissement et à la dégradation des aliments.
Pour lutter face à ces radicaux libres, il existe cependant des espèces appelées antioxydants. Ces espèces vont ainsi se réduire avec les radicaux libres, annihilant alors leurs actions. Nous verrons cependant ce processus plus en détail dans la partie sur comment empêcher le brunissement des fruits. Nous avons en effet réalisé des expérimentations sur le jus de citron, pour comprendre quelles espèces permettent d’arrêter l’oxydation.
On peut cependant dès maintenant noter que la vitamine C et la vitamine E sont deux antioxydants présents naturellement dans la pomme et la banane. La banane contient par contre 1.17mg de vitamine C pour une masse de 10g, et la pomme n’en contient que 0.46mg. La banane comporte aussi plus de vitamine E que son amie la pomme, avec 0.029mg contre 0.018mg, pour des masses de 10g de fruit une nouvelle fois. Ces différences notables de concentration en antioxydants, permettent d’expliquer le fait que lors de nos expériences nous avons constaté un brunissement plus prononcé de la pomme, et plus prononcé de la banane.
 Les fruits, et notamment le kiwi, sont riches en antioxydants. Ceux-ci lutte donc mieux face à l'action des radicaux libres, et nous permettent aussi à leur ingestion de réduire l'action des radicaux libres dans notre corps.
Credit Photographique : www.diabetendurance.org/antioxydant.html [Lien]
Les fruits, et notamment le kiwi, sont riches en antioxydants. Ceux-ci lutte donc mieux face à l'action des radicaux libres, et nous permettent aussi à leur ingestion de réduire l'action des radicaux libres dans notre corps.
Credit Photographique : www.diabetendurance.org/antioxydant.html [Lien]
Maintenant que nous avons introduits l’oxydation et les radicaux libres, avec un petit morceau sur les antioxydants, nous pouvons nous intéressent au phénomène du brunissement en lui-même.
II. Le processus d’oxydation du fruit
1. Le brunissement enzymatique
Au sein des fruits, on observe premièrement la présence de phénols (de formule brute C6H6O, mais dont on retrouve plusieurs isomères au sein du fruit), contenus à l’intérieur des cellules dans la vacuole, un organite présent dans les cellules végétales.
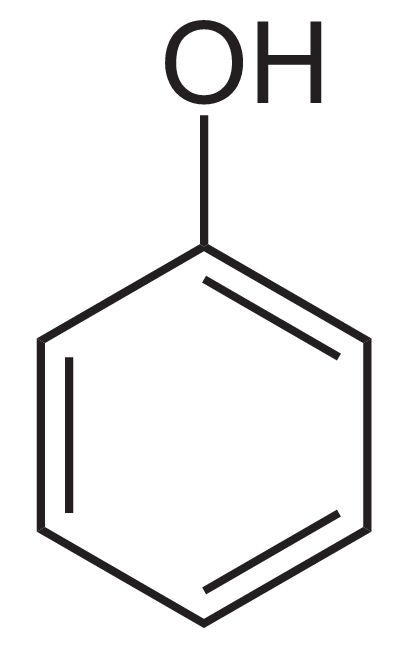 Un exemple de formule topologique d'un phénol.
Un exemple de formule topologique d'un phénol.
La cellule du fruit comporte aussi une enzyme du nom de polyphénoloxydase (abrégée PPO), qui est quant à elle contenue au sein du cytoplasme, tous deux séparés d’une fine membrane. Ce sont ces deux éléments qui vont rentrer en jeu dans le brunissement de la pomme, ainsi que le phénomène d’oxydation des phénols.
Une première expérience que nous avons réalisé et qui est assez simple est de couper une pomme en morceaux, et d’en laisser un morceau, placé sur une assiette, à l’air libre, pendant une heure entière. A la fin de l’heure, nous constatons sur la pomme un brunissement de la chair.

 Nous constatons sur ces photographies un brunissement du fruit au bout d'une heure. Nous allons désormais expliquer pourquoi ce phénomène se produit.
Nous constatons sur ces photographies un brunissement du fruit au bout d'une heure. Nous allons désormais expliquer pourquoi ce phénomène se produit.
En effet, lorsque l’on coupe le fruit, ou bien que celui-ci a simplement été écrasé, un processus commence à se réaliser à l’échelle cellulaire. La membrane séparant l’enzyme polyphénoloxydase des phénols est effectivement sectionnée, et ces deux éléments vont alors se mélanger et vont réagir ensemble. Si les phénols se trouvent au contact de l’air, l’enzyme va alors jouer le rôle de catalyseur de l’oxydation, et ceux-ci, par l’action de l’oxygène, vont s’oxyder en quinones.
Les quinones sont des molécules possédant une série de diènes (des molécules d’hydrocarbure avec 2 doubles liaisons), à la place des composés aromatiques. Ceci explique en partie la perte de goût du fruit. Il s’agit du réducteur qui s’est formé après l’oxydation des phénols, l’oxydant étant le dioxygène contenu dans l’air.
Les quinones ainsi formés vont eux-mêmes s’oxyder au contact du dioxygène sans avoir besoin d’enzymes particulières pour catalyser la réaction, et ils vont alors se polymériser en mélanine, un pigment brun que l’on retrouve chez l’Homme par exemple, et qui est à l’origine du brunissement des fruits. Ce brunissement du fruit est très perceptible, notamment chez la pomme.
Ainsi, plus schématiquement, l’oxydation du fruit comporte 3 étapes principales : Nous avons tout d’abord les phénols, contenus au sein des cellules, qui entrent en contact avec la polyphenoloxydase, à cause de la destruction de la membrane. Si les phénols sont en contact avec l’air, les phénols vont s’oxyder premièrement en quinones et qui à leur tour vont s’oxyder en mélanine, responsable du brunissement du fruit.
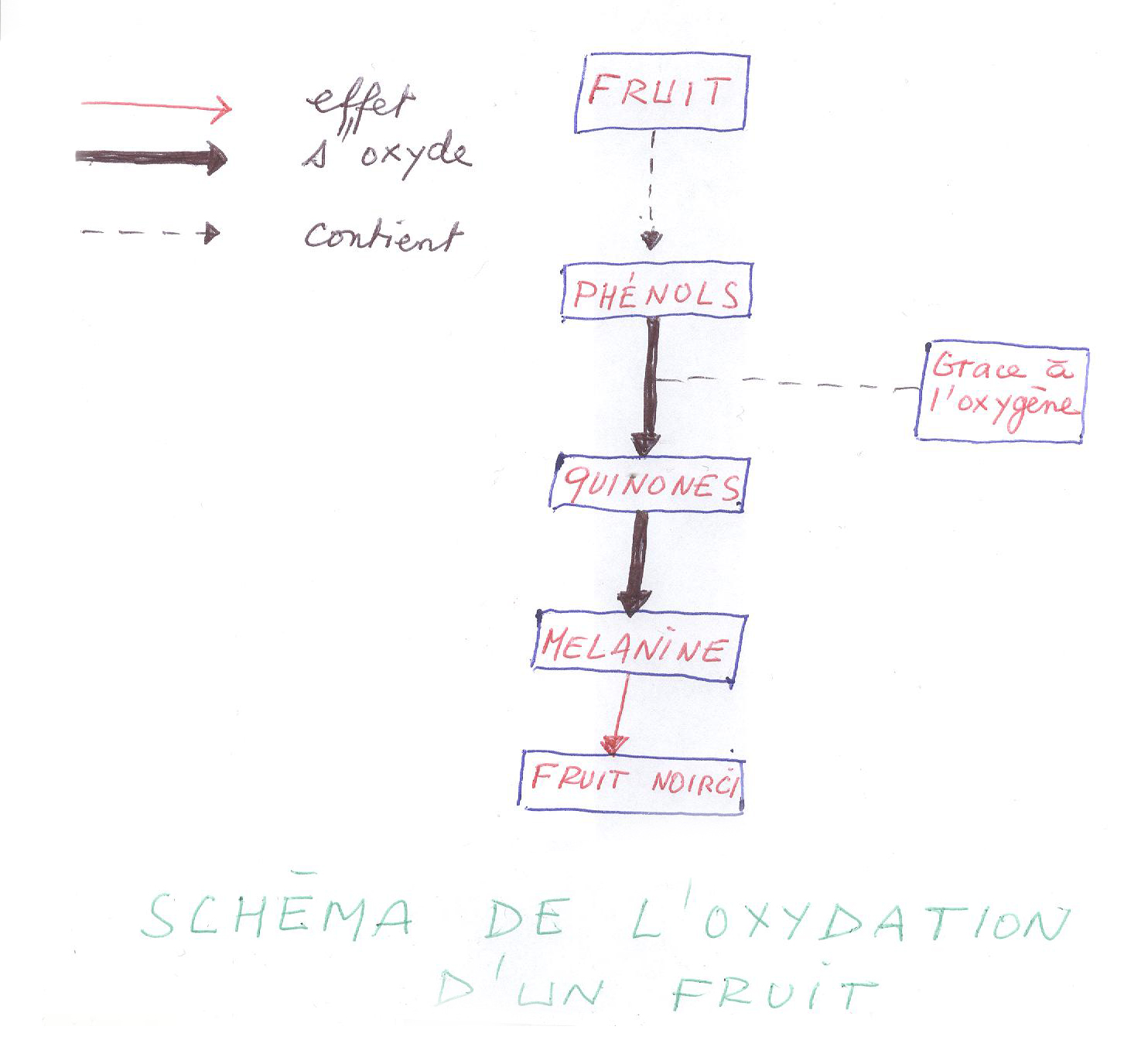 Schéma bilan de l'oxydation d'un fruit.
Schéma bilan de l'oxydation d'un fruit.
Ce phénomène constaté est appelé brunissement enzymatique, de par l’action de l’enzyme au sein du phénomène, accélérant la réaction d’oxydation. Ce changement d’aspect s’accompagne d’une modification du goût, celui-ci étant dégradé, car les mélanines sont des espèces non aromatiques.
Cependant, d’autres catalyseurs que l’enzyme présente au sein du fruit, c’est à dire des éléments étrangers à la réaction, mais qui contribuent à l'accélérer, entrent parfois en jeu, notamment dans l’environnement.
2. Catalyseurs de l’oxydation des fruits
L’enzyme présente au sein des cellules du fruit n’est pas le seul catalyseur de l’oxydation des phénols. Certains paramètres environnementaux favorisent en effet l’oxydation de ceux-ci. Nous avons donc cherché à déterminer quels sont ils par une série d’expérimentations similaire à celle réalisée sur les moisissures. Voici donc cette suite d’expériences.
Problème : Quels sont les facteurs qui favorisent, ou bien défavorisent le brunissement d’un fruit ?
Hypothèses : Placer un fruit dans un climat assez chaud, dans un milieu acide ou dans un milieu à la lumière favoriserait le brunissement du fruit, en catalysant notamment le processus d’oxydation.
Liste de matériel : A ajouter.
Protocole expérimental :
- - Nous découperons une masse de 10g de pomme ainsi qu’une masse de 6.6g à 6.7g de banane.
- - Nous placerons ensuite chacun de ces morceaux de fruits dans une assiette chacun, propre et étiquetée, selon le paramètre que nous testerons sur le fruit, dont la liste est la suivante :
- - La lumière.
- - L’obscurité.
- - Température faible de 4°C
- - Température plus élevée de 29°C
- - Milieu sous vide (De nouveau, la cloche sous vide était fissurée.)
- - Liquide à pH 4.0
- - Liquide à pH 7.0
- - Liquide à pH 9.0
- - En présence de sucre
- - En présence de sel
- - Nous laisserons ensuite ces fruits pendant 1 heure, et nous viendrons récupérer les résultats des expériences à la fin de ce décompte.
Résultats des expériences :
On constate tout d’abord une différence flagrante sur le brunissement entre pommes et bananes. Le brunissement des bananes est très léger comparé à celui de la pomme qui est prononcé et se voit au premier coup d’oeil.
A la lumière d’abord, on observe un brunissement relatif du fruit qui est plus important qu’à l’obscurité.

 On constate, même si ceci est assez difficile sur la banane, que la lulière favorise le brunissement du fruit, en son centrer.
On constate, même si ceci est assez difficile sur la banane, que la lulière favorise le brunissement du fruit, en son centrer.

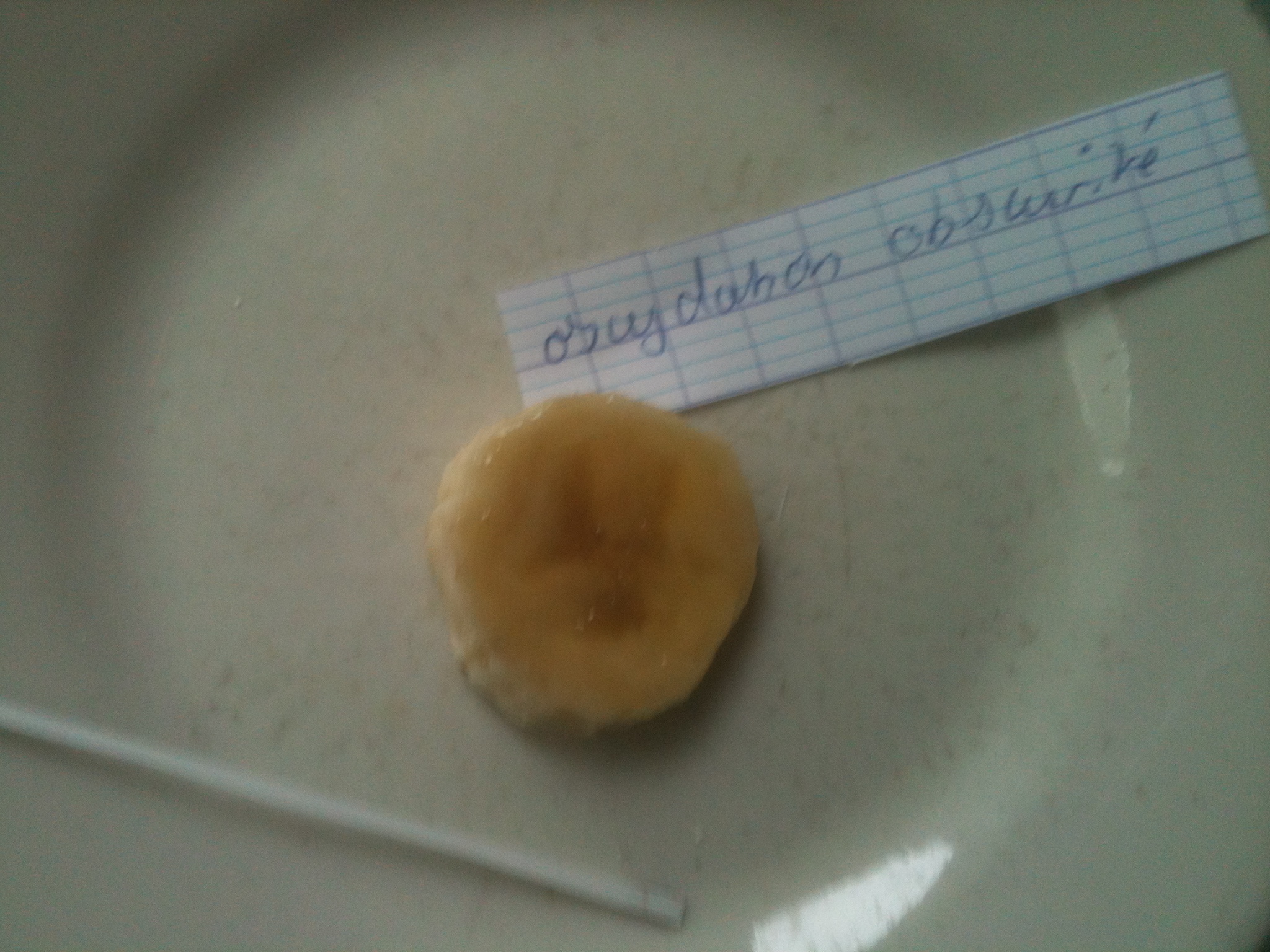 L'obscurité, au contraire de la lumière, favorise relativement moins l'oxydation des phénols.
L'obscurité, au contraire de la lumière, favorise relativement moins l'oxydation des phénols.
Pour une température faible de 4°C, on constate une oxydation faible des composés phénoliques, alors qu’à une température plus élevée, le brunissement est plus important, et se répartit à la surface du fruit.

 Des températures plus élevées, par contre, favorise le brunissement du fruit. (Le changement d'assiette est dû à un petit incident, quelqu'un ayant accidentellement fait tomber l'assiette précédente).
Des températures plus élevées, par contre, favorise le brunissement du fruit. (Le changement d'assiette est dû à un petit incident, quelqu'un ayant accidentellement fait tomber l'assiette précédente).
Une nouvelle fois, nous n’avons pas pu réaliser l'expérience sous vide, mais dans un tel milieu, le fruit ne s’est pas oxydé d’après les photographies que nous avons trouvé sur internet.
On remarque aussi que à un pH acide de 4.0, le fruit prend une couleur marron assez foncée, et ce de façon presque homogène sur l’ensemble du fruit. Pour un pH neutre de 7.0, l’oxydation est un peu moins poussée. Enfin, à un pH de 9.0, le brunissement est encore moins présent.

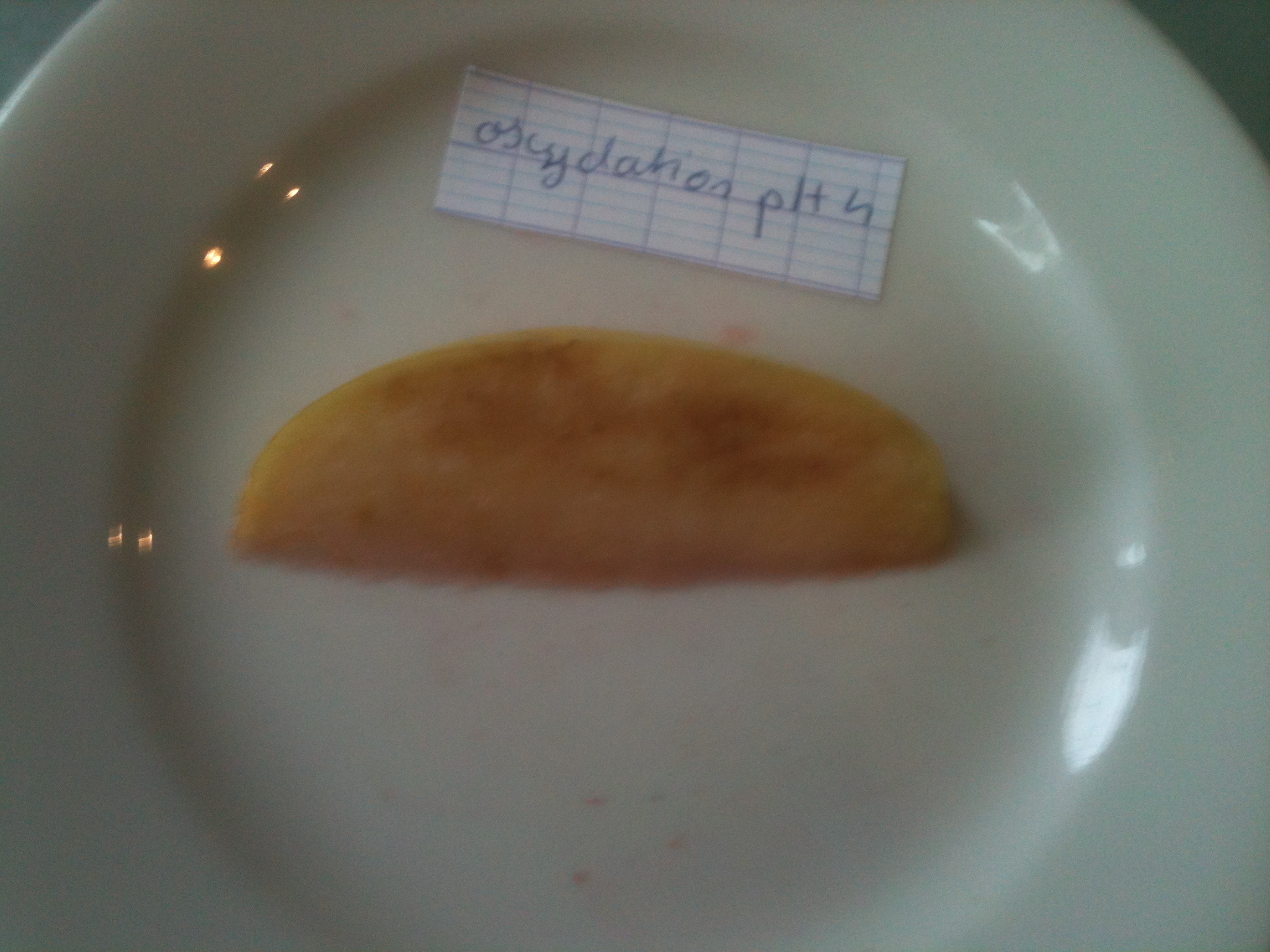 A un pH acide, le fruit présente un brunissement assez important à sa surface.
A un pH acide, le fruit présente un brunissement assez important à sa surface.

 A un pH neutre, le brunissement du fruit est moins important que pour un milieu acide.
A un pH neutre, le brunissement du fruit est moins important que pour un milieu acide.

 Enfin, avec un pH basique, le brunissement du fruit est encore moins prononcé.
Enfin, avec un pH basique, le brunissement du fruit est encore moins prononcé.
Finalement, en présence de sucre sur la surface du fruit, le brunissement est très léger, et il en est de même en présence de sel. où le brunissement est même quasi inexistant.

 En présence de sucre, le brunissement du fruit est amoindri.
En présence de sucre, le brunissement du fruit est amoindri.

 Les observations que l'on fait en présence de sel sont les mêmes qu'en présence de sucre.
Les observations que l'on fait en présence de sel sont les mêmes qu'en présence de sucre.
Ces constats s’expliquent de plusieurs façons. Généralement, certains facteurs environnementaux jouent sur la création de radicaux libres, augmentant ainsi le nombre de dégradation du fruits sur un même laps de temps. Les conditions du milieu dénaturent aussi parfois l’enzyme, changeant ainsi son fonctionnement.
Tout d’abord, le fait que la banane se soit moins brunie dans l’ensemble des expériences, vient du fait, comme déjà expliqué, que celle-ci est plus riche en antioxydants, limitant alors l’effet des radicaux libres formés par l’oxydation.
Le favoritisme de l’oxydation à la lumière vient de la présence de radiations ultraviolettes au sein du rayonnement, qui favorisent la formation de radicaux libres au sein du fruit, et donc favorise par la suite la création de mélanine. Ce fruit s’en trouve donc plus bruni qu’à l’obscurité, où le fruit s’est bruni de façon “normale”, puisque aucun autre paramètre n’est venu influencer la cinétique du brunissement, c’est à dire la vitesse du brunissement.
Le ralentissement du phénomène de l’oxydation au froid trouve quant à lui son explication dans le fait que le froid vienne inhiber l’action des enzymes. L’enzyme ne peut alors plus catalyser la réaction d’oxydation, et donc moins de quinones se forment, résultant d’une réduction de mélanine au sein du fruit.
A une température plus forte cependant, c’est l’élévation de la température qui favorise la formation de radicaux libres comme en présence de rayons ultraviolets, et ainsi les réactions en chaînes s’accumulent renforçant donc le brunissement du fruit.
L’absence d’oxydation du fruit sous vide est quant à elle plus simple à expliquer. En effet, l’oxydation nécessitant présence de dioxygène pour se réaliser, et puisqu’un milieu sous vide ne comporte plus ce dioxygène, il est impossible donc que le fruit brunisse, le phénomène d’oxydation n’ayant pas lieu.
Nous savons que plus un milieu est basique, plus celui-ci comporte d’ions OH-. Cette solution de plus en plus basique possédant donc de plus en plus d’ions hydroxyle a la possibilité de céder plus d’électrons aux radicaux libres (les ions OH- possèdent une charge négative excédentaire), et en cédant ces électrons, cette solution vient contrer les radicaux libres, permettant ainsi de limiter de plus en plus le brunissement du fruit. Ainsi, plus le pH augmente, plus la concentration en ions OH- augmente, et moins le nombre de radicaux libres est important. Le brunissement en est donc moins important.
Enfin, comme pour les moisissures, les enzymes ont besoin d’une certaine activité de l’eau (Aw) pour avoir un fonctionnement normal. Tant que l’Aw ne descend pas en dessous du seuil de 0.3, l’enzyme aura un fonctionnement. Cependant, moins l’activité de l’eau est importante et moins son fonctionnement sera prononcé. Ainsi, comme on le verra plus en détail dans la partie sur la lutte contre les moisissures, l’ajout de sucre et de sel réduit l’activité de l’eau (agents dépresseurs). L’activité de l’eau étant réduite, l’action de l’enzyme est réduite, et l’oxydation est moins importante.